El papel del potencial mixto en la separación selectiva de enargita y calcopirita con IPETC
Por: Isabel Lázaro1, Rubicelia García-Garnica2, Roel Cruz1,2
Resumen
Se presenta un estudio que resalta la importancia de considerar que el potencial que experimenta una superficie mineral bajo condiciones oxidantes (potencial mixto) no es equivalente al potencial que se registra en una solución o pulpa con el oxidante disuelto, mediante un electrodo de platino (ORP). Esto es particularmente importante en procesos como el de flotación, en el que se aprovecha esta condición para hacer una separación selectiva de minerales. Como caso de estudio, se presentan resultados de un análisis electroquímico de superficies de enargita (Cu3AsS4) y calcopirita (CuFeS2), antes y después de ser oxidadas con hipoclorito de sodio (NaClO) y el efecto que esto tiene en la interacción de estas superficies con el colector O-isopropil-N-etil tiono-carbamato (IPETC). Se encontró que el uso de NaClO a un pH de 10 genera un potencial mixto en la superficie de enargita y calcopirita que hace que la superficie de enargita esté en una condición más oxidante que la calcopirita. Asimismo, las condiciones oxidantes a este potencial promueven la formación de especies químicas en las superficies de estos minerales, que favorecen más la adsorción del colector en enargita. Cinéticas de adsorción sobre la enargita oxidada mostraron que la adsorción de IPETC es mayor en ésta que en la calcopirita, lo cual se sugiere es debido a la generación de un mayor número de sitios de interacción para la enargita. Sin embargo, los resultados indican también que, aunque es mayor la adsorción, la velocidad de este proceso es más baja, lo cual podría ser una desventaja en los tiempos cortos de contacto que se dan en la flotación.
Summary
This work highlights the importance of the so-called mixed potential, which represents the potential achieved on a mineral surface that is different to that expe-rienced by a platinum electrode in the same medium under oxidizing conditions. Establishing this value is important as it defines conditions that help promote selectivity in the process of flotation of minerals. In this work, an electrochemical analysis of enargite (Cu3AsS4) and chalcopyrite, before and after being exposed to an oxidizing reagent such as sodium hypochlorite (NaClO) was carried out. The study also involved studying the effect of the products of oxidation on the interaction with the collector used, IPECT. The results showed, that NaClO at a pH of 10 produces a higher mixed potential for enargite than for chalcopyrite. Likewise, the oxidizing conditions at this potential promote the formation of chemical species on the enargite surface that favor adsorption of the collector. Analysis of the adsorption kinetics of IPETC for both minerals, showed a higher adsorption of collector on enargite, which is associated to a higher number of interaction sites for enargite. Nevertheless, the results also indicate that despite a higher and more favored adsorption on enargite, it presents slow kinetics, and this could be a disadvantage given the short time of contact involved in the flotation process.
Introducción
El control de las condiciones oxidantes o reductoras de un sistema, es algo que invariablemente está asociado a la medida de un potencial redox, comúnmente denominado ORP (por las siglas en inglés para oxidation-reduction potential). En este sentido se ha asumido tácitamente o de manera equivocada que el potencial medido en solución o en una pulpa mediante un electrodo inerte como platino, es idéntico al que experimenta una superficie mineral (potencial mixto) en el mismo medio (Nicol y Lázaro, 2002). Esto cobra particular relevancia cuando se considera como parámetro de control de un proceso como, por ejemplo, la flotación selectiva de un mineral. En este tipo de procesos se parte de la premisa de poder separar minerales por flotación promoviendo condiciones hidrofóbicas en el mineral a flotar y condiciones hidrofílicas en el o los minerales a deprimir (Guo y Yen, 2005; Lattanzi et al., 2008).
Para este propósito se toman como parámetros de control el pH y el ORP de la pulpa, este último controlado mediante la adición de agentes oxidantes reductores (Fornassiero et al., 2001; Bruckard et al., 2010). En muchos estudios, sin embargo, se pierde de vista que el papel de un agente oxidante o reductor va más allá de fijar un potencial redox en solución, y sobre todo que el potencial medido en la pulpa por una sonda formada por un electrodo de platino y uno de referencia, es diferente al potencial mixto desarrollado entre la solución y la superficie mineral.
En un estudio reciente, García-Garnica et al. (2022) demuestran la importancia de hacer esta consideración y establecen que en el caso de minerales como enargita (Cu3AsS4) y calcopirita (CuFeS2) se registran diferentes valores de potencial mixto (Em), aunque se use el mismo agente oxidante bajo las mismas condiciones experimentales. Asimismo, reportan que hay transformaciones de la superficie mineral que son función del agente oxidante empleado. A partir de analizar varios agentes oxidantes, estos autores concluyeron que el hipoclorito de sodio (NaClO) podría ser muy útil en el manejo adecuado de ORP como parámetro de control en un proceso de flotación de sulfuros de cobre.
El objetivo del presente trabajo es evaluar el efecto del Na-ClO para favorecer una separación selectiva entre enargita y calcopirita bajo condiciones de flotación utilizando un colector específico para especies de cobre tipo tionocarbamato (IPETC) que de acuerdo con reportes en la literatura permite tener recuperaciones de enargita mayores a 80% (Castro et al., 2003). Los resultados generan conocimiento orientado al desarrollo de un proceso de separación de sulfosales (Cu3AsS4) de sulfuros de cobre (CuFeS2), cuya relevancia se deriva de las limitaciones que impone el contenido de arsénico (<0.2%) a la comercialización de concentrados de cobre (Agorhom et al., 2015).
Metodología
Para este estudio se emplearon muestras minerales de Cu3AsS4 y CuFeS2, provenientes de los depósitos Leonard en Montana y Charcas en San Luis Potosí, respectivamente. Mediante análisis de difracción de rayos X con un equipo Bruker DaVinci 8, se encontró que las muestras eran de alta pureza, pero debido al límite de detección de esta técnica, se realizó análisis químico que reveló una pureza de 96 y 98% para Cu3AsS4 y CuFeS2, respectivamente.
Para realizar análisis electroquímico y medidas de potencial, se prepararon electrodos siguiendo lo descrito en (García-Garnica et al., 2022) y se utilizó un sistema convencional de tres electrodos que involucraba un potenciostato /galvanostato 3F VersaS-TAT controlado por el software VersaStudio®, mediante el cual se evaluó la zona de potencial relevante, que fue establecida mediante mediciones de potencial en presencia (Em) y ausencia de hipoclorito de sodio (NaClO) como agente oxidante.
En todas las pruebas se empleó una concentración 0.003 M de NaClO que fue la que produjo los valores más altos de potencial mixto para Cu3AsS4.
Por otro lado, para el control de pH se consideró un sistema de solución buffer borato/hidróxido de sodio que permitió fijar el pH en un valor de 10.
Asimismo, se empleó como colector IPETC, cuya adsorción a Cu3AsS4 y CuFeS2, fue evaluada indirectamente mediante la determinación de la cantidad de IPETC remanente en solución, posterior a su interacción con estos minerales. Para la determinación de IPETC se realizaron mediciones de UV a una longitud de onda de 291.5 nm usando un equipo UV vis Thermo Scientific Genesys 10s. Se realizaron pruebas de microflotación de enargita en un tubo Hallimond modificado para la inyección de gas nitrógeno, se utilizó 1.0 g de mineral, la pulpa se acondicionó previamente con NaClO, posteriormente se agregó el colector a una concentración de 1×10-4 M, se colocó en el tubo y se flotó durante 1 minuto.
Resultados
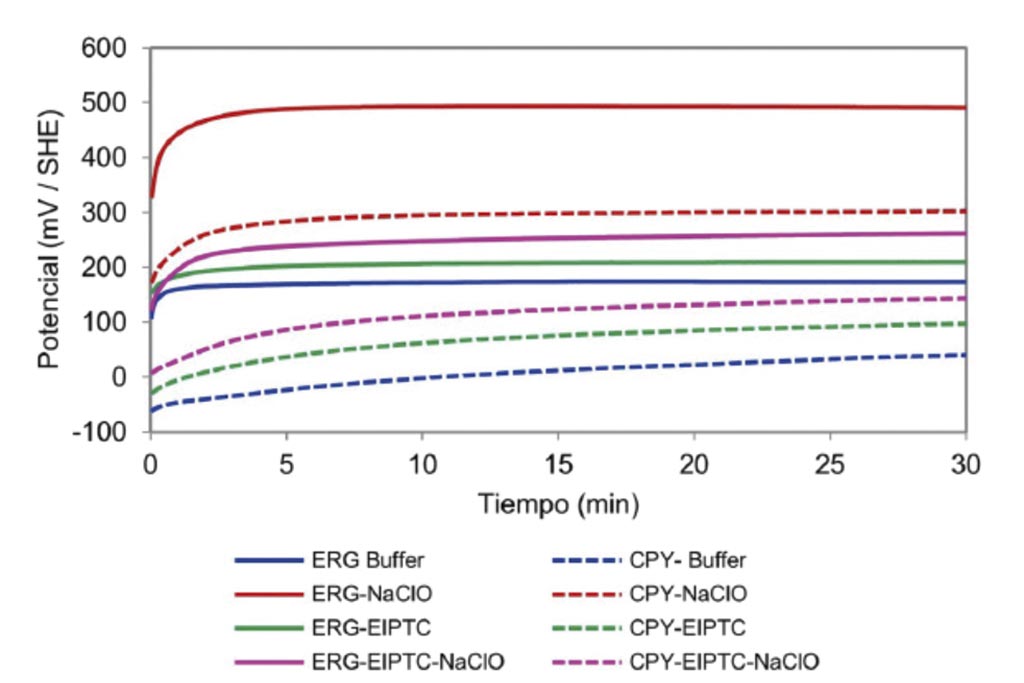
En la Figura 1 se resumen resultados de mediciones de potencial realizadas con electrodos de enargita y calcopirita en solución buffer conteniendo o no IPETC en presencia y ausencia de agente oxidante. Para ambos minerales, el potencial es más positivo en presencia de NaClO, particularmente para enargita. Cuando se adiciona el colector se observa una disminución en el potencial, lo que indica que el IPETC se está adsorbiendo en la superficie mineral, y resulta en la inhibición de las reacciones de oxidación de ambos minerales. Dada la diferencia de potencial que se genera entre enargita y calcopirita en todas las condiciones evaluadas, se puede considerar que es posible tener selectividad entre estas especies en el proceso de flotación. Esto confirma la importancia de establecer el valor de potencial que registra la superficie mineral. Así entonces, se establece que la zona de potencial relevante está entre 0 y 500 mV.
Con el objetivo de conocer el comportamiento electroquímico del colector, se obtuvieron voltamperogramas cíclicos de electrodos de enargita y calcopirita en el medio buffer en presencia y ausencia de colector. Para descartar reacciones propias del medio y del IPETC, se obtuvieron voltamperogramas usando un electrodo de platino, el cual es inerte en el intervalo de potencial a evaluar (Figura 2). Así entonces, se encontró que el medio presenta una ligera oxidación en la zona de potencial de interés y que el colector sufre reducción a potenciales menores de 0 mV, lo cual está por debajo de la zona de interés.
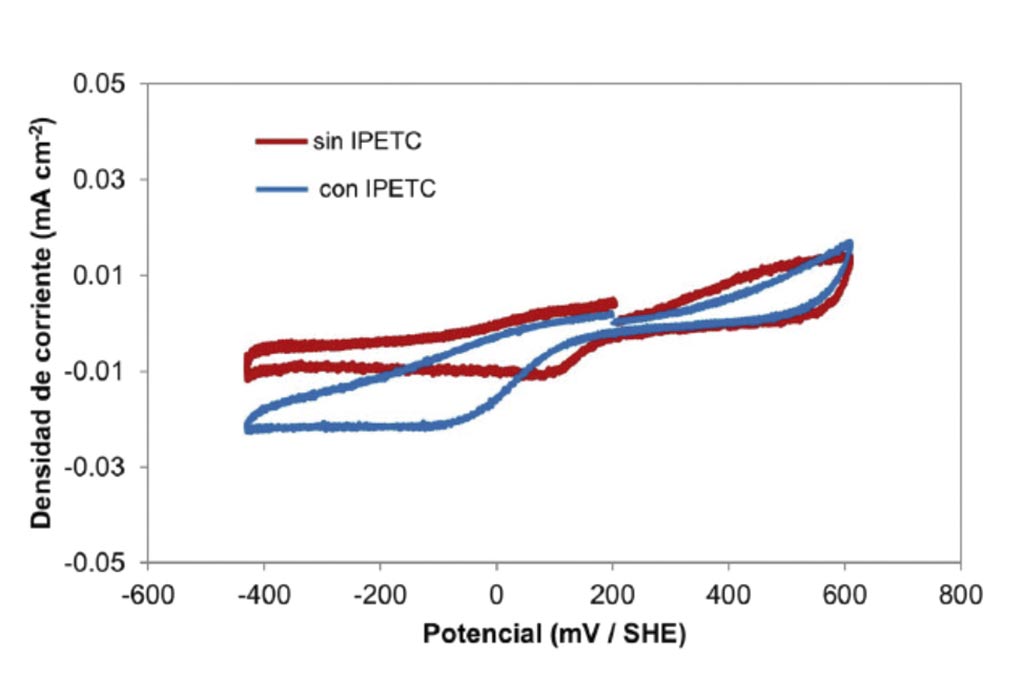
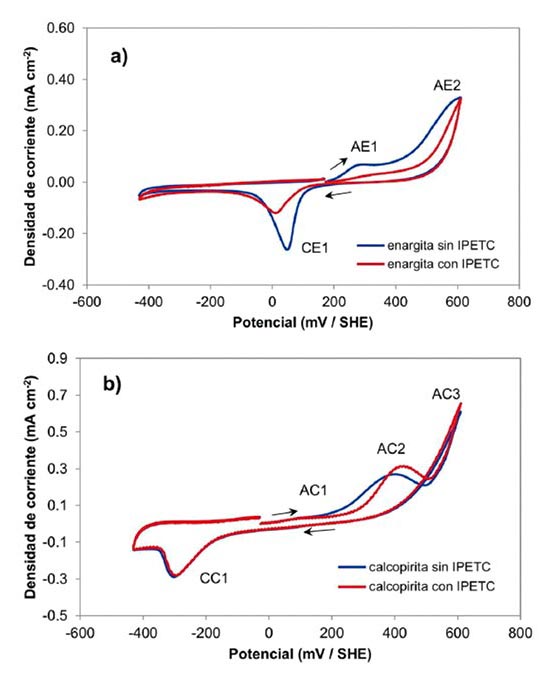
Figura 3. Voltamperogramas de enargita (a) y calcopirita (b), en ausencia y presencia de colector IPETC (1X10-4 M), pH 10, velocidad de barrrido 5 mV/s. La exploración se inició desde el potencial de equilibrio hacia la dirección positiva.
La respuesta electroquímica de enargita (Figura 3a) en ausencia de IPETC está caracterizada por dos procesos de oxidación etiquetados como AE1 y AE2, así como un proceso de reducción CE1, de acuerdo con lo reportado por García-Garnica et al. (2022), cada una de estas señales electroquímicas se atribuyen a las reacciones 1 a 4.
(AE1) Cu3AsS4 + 2xOH– —> Cu3-xAsS4 + xCu(OH)2 +2xe– 1
(AE2) Cu3-x AsS4 +(10 – 2x)H2O —> (3-x)Cu(OH)2 + HAsO42- + 4S2- +(13 -2x)H+ +(3-2x)e- 2
(CE1) 2Cu (OH)2 + 2e- —->Cu2O + 2OH– + 2H2O 3
(CE1) HAsO42- + 2e– + 2H+ —-> HAsO2-3 + H2O 4
De igual manera, la calcopirita involucra tres procesos de oxidación AC1, AC2 y AC3, así como un proceso de reducción CC1 (Figura 3b), que están representados por las siguientes reacciones 5 a 8.
(AC1) 2CuFeS2 + 6xOH– –> 2CuFe1-x S2 + xFe2O3 + 3xH2O +6xe– 5
(AC2) CuFeS2 + 3OH– —> CuS+2 + Fe (OH)3 + 3e– 6
(AC3) CuS+2+2OH– —> Cu(OH)2 + 2S + 2e– 7
(CC1) Cu(OH)2 + S + 2e– —> CuS + 2OH– 8
Se observó que en presencia de colector hay una disminución en la corriente asociada al proceso AE1 y que se mantiene en AE2, como resultado de la interacción electroquímica del mineral con el colector a pH 10. Esto se puede interpretar como la formación de una película generada por la adsorción de colector en la superficie de Cu3AsS4 (Flores-Alvarez et al., 2017), lo cual generaría una superficie hidrofóbica. La adsorción de IPETC en enargita pasiva la oxidación del mineral, por lo que esto afecta el proceso catódico CE1, representado como una disminución de la densidad de corriente asociada.
Por otro lado, en el caso de calcopirita la adsorción de colector no está favorecida ya que la respuesta en corriente es prácticamente la misma en ausencia y presencia de colector (Figura 3b). Las ligeras variaciones en potencial y corriente de AC2, podrían indicar una ligera adsorción del colector pero que, en comparación con enargita, no logra inhibir la oxidación al incrementar el potencial. Esto confirma que la enargita en medio alcalino presenta una mayor adsorción de IPETC que la calcopirita lo cual puede favorecer la selectividad de flotación entre estas especies.
Con el fin de comparar el efecto de interacción del colector con superficies de mineral previamente oxidadas, se obtuvieron voltamperogramas de mineral previamente oxidado con NaClO y se evaluó su interacción con IPETC bajo estas condiciones. En la polarización anódica de enargita (Figura 4a) se puede observar un incremento en el potencial de inicio, lo que está en línea con las medidas de potencial mixto (Figura 1), y una disminución de corriente en comparación con la polarización anódica de enargita en el medio buffer. Lo anterior, se puede interpretar como un efecto importante de la oxidación química en la adsorción del colector, ya que el tratamiento inicial parece inhibir la adsorción o favorecer que esta se realice sobre la superficie que no participa en el proceso anódico, ya que el proceso de oxidación asociado al pico AE1 es remplazado por la oxidación química, por lo que ya no aparece, mientras que el pico AE2 presenta un incremento en la densidad de corriente.
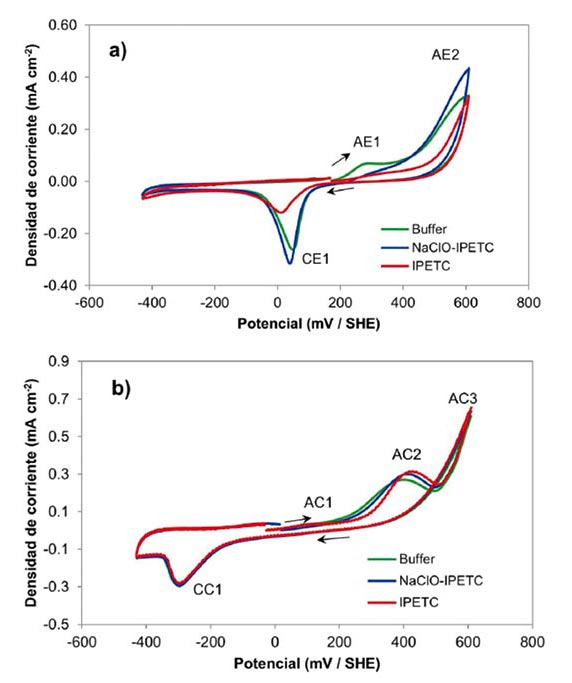
En el caso de calcopirita nuevamente se evidenció que no hay diferencias significativas en la señal electroquímica registrada (Figura 4b). Al comparar la respuesta de calcopirita previamente oxidada en presencia de IPETC con la calcopirita en el buffer, se puede observar solo un ligero desplazamiento en potencial de CA2, esto sugiere que existe una ligera adsorción de colector en la superficie de calcopirita, lo cual genera un desplazamiento en el potencial asociado a este proceso. Los resultados sugieren que el agente oxidante NaClO tiene la capacidad de generar una selectividad entre los minerales estudiados, ya que la adsorción de IPETC en calcopirita sería menor que la que pudiera alcanzar en la superficie de enargita, por lo que esta puede ser más susceptible de incrementar su hidrofobicidad y por ende, tener una mayor capacidad de flotación que la calcopirita bajo las condiciones experimentales estudiadas.
Para fortalecer los resultados del estudio electroquímico, se realizaron pruebas de adsorción en muestras de enargita y calcopirita sin oxidar a pH 10, usando una concentración de 1×10-4 M IPETC (Figura 5). Como se puede observar, el comportamiento de adsorción y su magnitud es diferente para cada mineral. La enargita presenta una mayor adsorción de IPETC, al adsorber 58 % más de colector que la muestra de calcopirita, lo cual sugiere que el porcentaje de recuperación de enargita podría ser mayor que el de calcopirita en el proceso de flotación bajo estas condiciones.
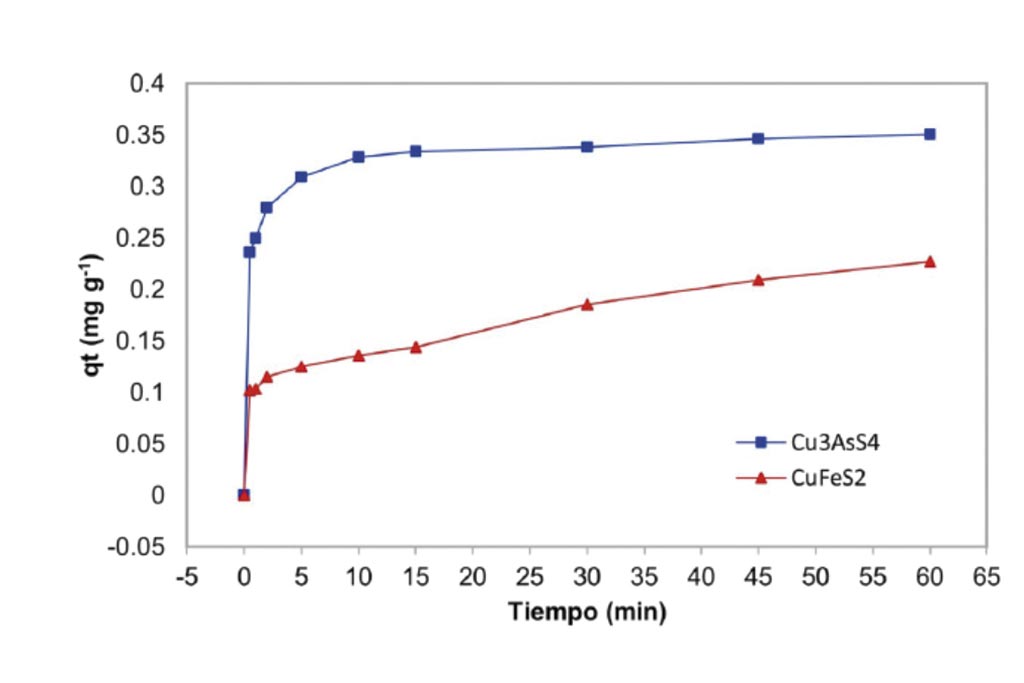
El tiempo de equilibrio, es decir, el tiempo que requiere la muestra mineral para adsorber la mayor cantidad de colector y a partir del cual no se observa un cambio relevante en la densidad de adsorción, fue de 10 min para la muestra de enargita, ya que a tiempos mayores la adsorción se incrementa de forma mínima. En el caso de la calcopirita se puede observar que a partir de 30 min la velocidad de adsorción empieza a disminuir, sin embargo, no alcanza el equilibrio en el tiempo estudiado, pese a esto, no se consideró aumentar el tiempo de evaluación de las cinéticas, debido a que en el proceso de flotación de minerales se utilizan tiempos de acondi-cionamiento menores a 20 min, y en este caso, se busca una flotación selectiva entre estos minerales, y una mayor velocidad de adsorción de colector en enargita favorece la selectividad, esperándose una mayor recuperación en el proceso de flotación con respecto a calcopirita, en la que se presenta un velocidad más baja de adsorción de IPETC.
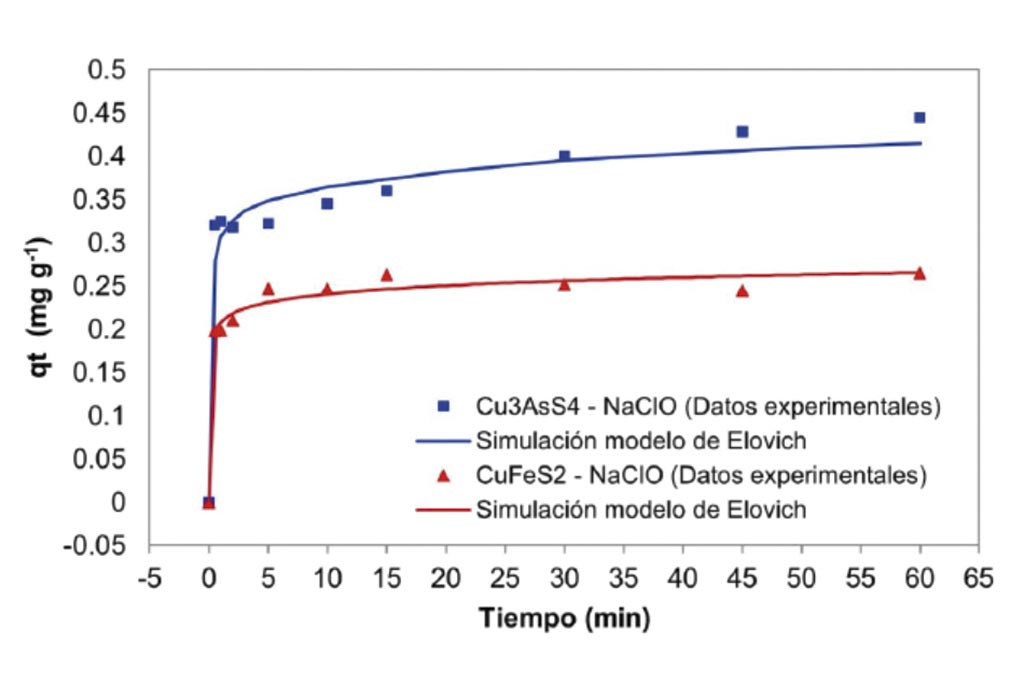
Figura 6. Densidad de adsorción de IPETC en enargita y calcopirita oxidadas con NaClO. Condiciones de experimentación: pH 10, [IPETC] = 1×10-4 M.
Para evaluar el efecto del agente oxidante en la adsorción de IPETC, se realizaron pruebas de adsorción con muestras preoxidadas de enargita y calcopirita. Los resultados de la Figura 6 muestran que hay una mayor cantidad de colector adsorbido en ambos minerales, sin embargo, el efecto en la cinética de adsorción parece ser mayor para la calcopirita. Como puede observarse, el retraso o baja adsorción observada, en los primeros 15 min, para la calcopirita sin oxidar desaparece después de ser tratada con NaClO. Por otro lado, una vez oxidada la enargita con NaClO, esta incrementa la adsorción de IPETC, pero ahora presenta una cinética más lenta en los primeros 5 min de equilibrio.
Se ha reportado que la adsorción de IPETC en sulfuros de cobre tiene lugar mediante un mecanismo de quimisorción y este mecanismo se ha caracterizado como una combinación de procesos químicos y electroquímicos dependiendo del potencial del sistema (Buckley et al., 2014). Cuando existe tal mecanismo, la reacción entre el anión IPETC y los átomos metálicos expuestos en la superficie de la red mineral da como resultado la formación de Cu(IPETC) (Güler et al., 2006).
Se ha reportado también adsorción preferente de IPETC sobre sitios de Cu con respecto a los sitios de Fe (Mkhonto et al., 2022). Por lo que, la estructura sin contenido de hierro de la enargita ofrecería una mejor superficie para la adsorción con respecto a la calcopirita que contiene tanto átomos de cobre como de hierro. Por otra parte, de acuerdo con las reacciones iniciales del proceso de oxidación de cada mineral, la generación de especies superficiales de cobre en enargita, ofrecería una mayor disponibilidad de sitios de adsorción para el IPETC que la calcopirita, ya que la disolución de cobre en este último mineral se da a potenciales más oxidativos con respecto a la enargita, que como se demostró, alcanza mayores potenciales para las condiciones de estudio. La formación de diferentes sitios de adsorción en ambos sistemas se revela con los respectivos retrasos en las cinéticas de adsorción, lo cual podría estar asociado a la formación de bicapas en función de la disponibilidad de sitios de adsorción para el IPETC.
Lo anterior es demostrado por los cálculos cinéticos, que muestran que la adsorción de IPETC en calcopirita se da a una mayor velocidad (44,496.58 mg g-1 min-1), que en enargita (3,045.74 mg g-1 min-1), ya que se favorece al generar sitios disponibles de cobre a los altos potenciales que alcanza el NaClO, pero al parecer en una menor cantidad por ofrecer menores sitios de adsorción (solo las especies oxidadas), con respecto a la enargita que parece presentar adsorción tanto en las especies oxidadas como en los sitios sin alterar.
Es importante señalar que aunque la oxidación con NaClO favorece una importante adsorción en la enargita, la mayor diferencia de adsorción se da hasta después de los 20 minutos de equilibrio, a diferencia del sistema sin oxidar en la que la mayor diferencia se da desde los primeros 5 minutos de equilibrio, lo que indica que es importante evaluar el efecto del control del potencial mixto a través del grado de oxidación con NaClO (tiempo de reacción) que permita definir las condiciones mas favorables.
Por lo anterior, se puede entender que en el caso de la enargita donde el cobre se oxida a una mayor velocidad, la interacción Cu-IPETC está más favorecida que en calcopirita, ya que el potencial que se establece en calcopirita promueve primero la salida del Fe (Ec. 5) de su estructura.
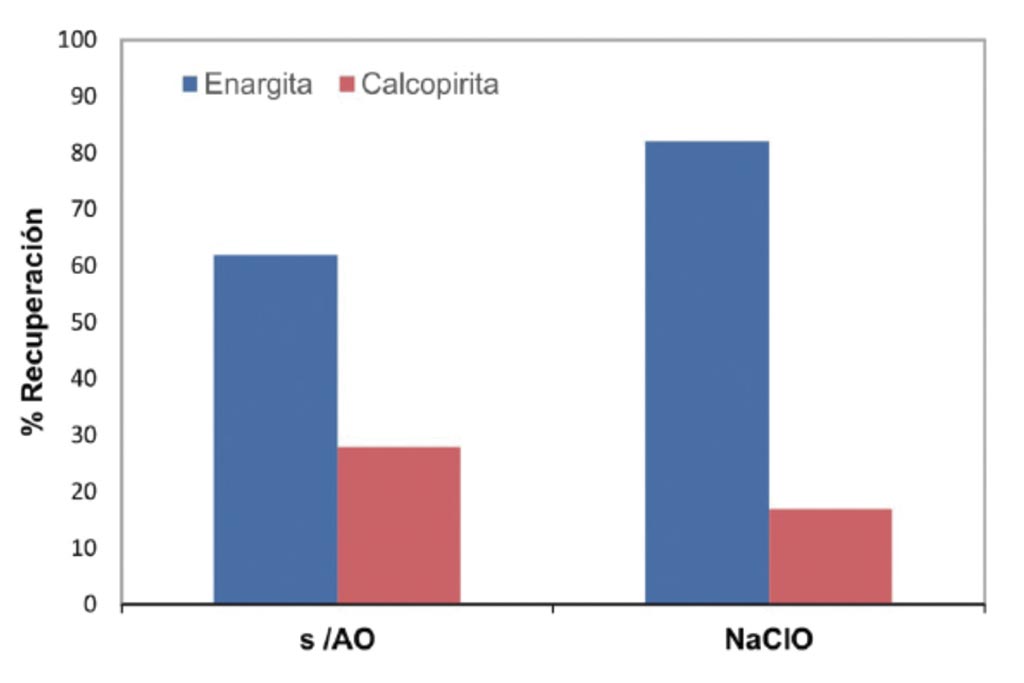
A fn de corroborar el efecto positivo del NaClO como medio de control del potencial mixto en el sistema, para la flotación selectiva de enargita sobre calcopirita, se realizaron pruebas de microflotación de estos minerales (Figura 7). Los resultados muestran que es posible establecer una selectividad de flotación, alcanzándose recuperaciones mayores a 80% de enargita y menores a 20% de calcopirita. Por lo que se comprueba lo inferido por el análisis de los resultados del estudio electroquímico y de adsorción de IPETC sobre los minerales de cobre bajo diferentes condiciones de estado superficial a través del control del potencial mixto.
Conclusiones
La combinación de estudios electroquímicos y de cinéticas de adsorción ofrecen una opción complementaria para el estudio de las interacciones entre colectores y superficies minerales bajo diferentes condiciones superficiales. De tal forma que fue posible inferir los factores que determinan la velocidad y el grado de adsorción del IPETC sobre minerales de cobre enargita y calcopirita. A partir de los resultados del estudio electroquímico se observó que la adsorción del colector tiene mayor efecto en el proceso oxidativo de la enargita que en la calcopirita, lo que es un indicio de que se da una adsorción preferente del IPETC sobre el primero. Cuando se ponen en contacto los minerales con NaClO, la superficie oxidada resultante del control del potencial mixto afecta el proceso adsorción para ambos minerales, observándose en primera instancia un incremento en el grado de adsorción para ambos minerales. No obstante, la adsorción sobre la enargita oxidada es mayor que la de la calcopirita, lo cual se sugiere es debido a la generación de mayor numero de sitios de interacción para la enargita. Sin embargo, los resultados indican que, aunque es mayor la adsorción, la velocidad de este proceso es mas baja, lo cual podría ser una desventaja en los tiempos cortos de contacto que se dan en la flotación. Resultados preliminares de microflotación, muestran que es posible generar selectividad y obtener una recuperación de enargita mayor de 80%, sin embargo, es necesario evaluar más ampliamente el efecto del grado de oxidación generado por el tiempo de contacto y concentración del NaClO.
Agradecimientos
Los autores agradecen a la Universidad Autónoma de San Luis Potosí por el apoyo financiero para este trabajo. Rubicelia García-Garnica agradece la beca 457718 otorgada por CONACYT. También se agradece el apoyo brindado por Martha Franco en los experimentos.
Referencias citadas
- Agorhom, E. A., Lem, J. P., Skinner, W. y Zanin, M. 2015. Challenges and opportunities in the recovery/rejection of trace elements in copper flotation-a review: Minerals Engi-neering, V. 78, p. 45–57.
- Bruckard, W. J., Davey, K. J., Jorgensen, F. R. A., Wright, S., Brew, D. R. M., Haque, N. y Vance, E. R. 2010. Development and evaluation of an early removal process for the beneficiation of arsenic-bearing copper ores: Minerals Engineering, V. 23, p. 1167-1173.
- Buckley, I. N., Hope G. A., Lee, K. C., Petrovic, E. A., Woods, R. 2014. Adsorption of O-isopropyl-N-ethyl thionocarbamate on Cu sulfide ore minerals: Minerals Engineering, V. 69, p. 120-132.
- Castro, S.H., Baltierra, L., Hernandez, C. 2003. Redox conditions in the selective flotation of enargite: Electrochemistry in Mineral and Metal Processing VI: Proceedings of the International Symposium. The Electrochemical society, V. 18, p. 27-53.
- Flores-Álvarez, J., Elizondo-Álvarez, M., Pulido, G., Guerrero-Flores, A. y Uribe-Salas, A. 2017. Electrochemical behavior of galena in the presence of calcium and sulfate ions: Minerals Engineering, V. 111, p. 158-166.
- Fornasiero, D., Fullston, D., Li, C., Ralston, J. (2001). Separation of enargite and tennantite from non-arsenic copper sulfide minerals by selective oxidation or dissolution. International Journal of Mineral Processing, V. 61(2), p. 109–119.
- Güler, T., Hiçyilmaz, C., Gökagˇaç, G. y Ekmeçi, Z. 2006. Adsorption of dithiophosphate and dithiophosphinate on chalcopyrite: Minerals Engineering, V. 19(1), p. 62-71.
- Guo, H. y Yen, W.T. 2005. Selective flotation of enargite from chalcopyrite by electrochemical control: Minerals Enginee-ring, V18(6), p. 605–612.
- García-Garnica, R., Castillo-Magallanes, N., Rodríguez, I., Cruz, R., y Lázaro, I. 2022, Electrochemical study of enargite within the mixed potential zone attained with different oxidizing reagents in an alkaline medium: Electrochimica Acta, V. 425, p. (140729)1-12.
- Lattanzi, P., Da Pelo, S., Musu, E., Atzei, D., Elsener, B., Fantauzzi, M. y Rossi, A. 2008. Enargite oxidation: A review. Earth-Science Reviews, V86(1–4), p. 62–88. Nicol M.J. y Lázaro, I. 2002, The role of EH measurements in the interpretation of the kinetics and mechanisms of the oxidation and leaching of sulphide minerals: Hydrometallurgy, V. 63(1), p.15–22.
- Peace P. Mkhonto, P. P., Xingrong Zhang, X., Liang Lu, L., Wei Xiong, W., Yangge Zhu, Y., Long Han, L., Phuti E. Ngoepe, P. E. 2022. Adsorption mechanisms and effects of thiocarbamate collectors in the separation of chalcopyrite from pyrite minerals: DFT and experimental studies: Minerals Engineering, V. 176, p. (107318)1-14.
- Nicol M.J., Lázaro, I. 2002. The role of EH measurements in the interpretation of the kinetics and mechanisms of the oxi-dation and leaching of sulphide minerals: Hydrometallurgy, V. 63(1), p.c 15–22.
1 Universidad Autónoma de San Luis Potosí, Instituto de Metalurgia, Av. Sierra Leona No. 550, Lomas 2a Sección, 78210 San Luis Potosí, SLP, México, ilazaro@uaslp.mx
2 Universidad Autónoma de San Luis Potosí, Facultad de Ingeniería, Dr. Manuel Nava No. 8, Zona Universitaria Poniente, 78290 San Luis Potosí, SLP, México.




















