Uso del biopolímero F-250 en la depresión selectiva de pirita: Estudios fundamentales y casos de estudio en la industria
Por: M. A. Corona Arroyo1, J. A. Ramos Guzmán2, D.M. Vargas2, A.N. Montero Gutiérrez1, M. Caudillo-Gonzalez1
Resumen
En los últimos años, lidiar con la pirita en los circuitos de flotación de galena, esfalerita y calcopirita se ha convertido en un desafío tanto en México como en el resto del mundo. La disminución en las leyes de cabeza de los minerales de valor ha obligado a las unidades mineras a procesar yacimientos con contenidos de hierro (Fe) más altos, superando el 20% de Fe, lo que dificulta el control del contenido de Fe en el concentrado. Además, estas altas leyes de Fe en la cabeza requieren el uso intensivo de cianuro de sodio y cal para la depresión del Fe presente.
En este trabajo de investigación, se presenta una evaluación fundamental y aplicada a nivel de laboratorio utilizando minerales provenientes de diferentes unidades mineras y reactivos orgánicos (biopolímero F-250) derivados de la lignina como una alternativa amigable con el medio ambiente para controlar el Fe en los circuitos de flotación de sulfuros. Se llevaron a cabo estudios de adsorción del biopolímero a base de lignina en la interfase de pirita/esfalerita/calcopirita y solución acuosa, y los resultados se relacionaron con estudios de microflotación. Una vez determinadas las condiciones de selectividad entre pirita, calcopirita y esfalerita, se realizaron pruebas de flotación a nivel de laboratorio para evaluar principalmente la dosificación del biopolímero, el tiempo de acondicionamiento y el pH de la pulpa.
Los resultados de la microflotación y la adsorción mostraron que los depresores de lignina presentan una excelente selectividad entre pirita, esfalerita y calcopirita, y se requieren dosis inferiores a 10 ppm en presencia de Xantato amílico de potasio. Además, se confirmó que el pH desempeña un papel crucial en el control de la adsorción y, por lo tanto, en la selectividad entre los minerales. En las pruebas de flotación de laboratorio, se logró una buena separación utilizando dosis de 5-50 g/tonelada para lograr una reducción de 3 unidades porcentuales en el grado final de Fe en comparación con el obtenido con cianuro de sodio. Por lo tanto, los biopolímeros de lignina representan una excelente alternativa para el control del Fe en los circuitos de flotación.
Palabras clave: Flotación, depresión de pirita, depresores orgánicos, pH bajos
Abstract
In recent years, dealing with pyrite in the flotation circuits of galena, sphalerite, and chalcopyrite has become a challenge both in Mexico and around the world. The decrease in the head grades of valuable minerals has forced mining units to process deposits with higher iron (Fe) contents, exceeding 20% Fe, making it difficult to control the Fe content in the concentrate. Moreover, these high Fe grades in the feed require intensive use of sodium cyanide and lime for the depression of the Fe present.
In this research work, a fundamental and applied evaluation at the laboratory level is presented using minerals from different mining units and organic reagents (F-250 biopolymer) derived from lignin as an environmentally friendly alternative for controlling Fe in sulfide flotation circuits. Adsorption studies of the lignin-based biopolymer at the pyrite/sphalerite/chalcopyrite-aqueous solution interface were conducted, and these results were correlated with microflotation studies. Once the selectivity conditions between pyrite, chalcopyrite, and sphalerite were determined, flotation tests were performed at the laboratory level, primarily evaluating the biopolymer dosage, conditioning time, and pulp pH.
The results of microflotation and adsorption showed that lignin depressants exhibit excellent selectivity among pyrite, sphalerite, and chalcopyrite, with dosages lower than 10 ppm being required in the presence of potassium amyl xanthate. Additionally, it was confirmed that pH plays a crucial role in controlling adsorption and, therefore, mineral selectivity. In laboratory flotation tests, a good separation was achieved using dosages between 5-50 g/ton to achieve a 3-percentage-point reduction in the final Fe grade compared to that obtained with sodium cyanide. Therefore, lignin biopolymers represent an excellent alternative for Fe control in flotation circuits.
Keywords: Flotation, pyrite depression, organic depressants, low pH
Introducción
La pirita es un sulfuro metálico que usualmente se considera como mineral de ganga debido a su bajo valor económico y suele presentar problemas en la separación de Pb, Cu y Zn. Dada su flotación con los minerales de valor, siempre se busca la forma de impedir su presencia en los concentrados de flotación de minerales y, por lo tanto, es procesado como material de desecho ( Wang & Forssberg, 1991). En las unidades mineras de México, se ha convertido en un problema cada vez más exigente, derivado del incremento en las leyes de hierro alcanzando valores del 20%. Sin embargo, a pesar de que suelen presentar una fácil liberación, ocasionan un incremento en el consumo de cianuro de sodio y cal para controlar su aparición en el concentrado final.
Debido a la facilidad con que la pirita puede flotar, en muchas ocasiones por el uso de colectores en el circuito de flotación para recuperar minerales de interés y dado que su flotación también se mejora mediante la activación de iones de cobre o plomo que emanan de otros minerales, se requieren reactivos para deprimir selectivamente la pirita. La flotación de pirita de forma no deseada trae consigo varias consecuencias como: (1) diluir el grado del concentrado y reducir el valor económico (Wang & Forssberg, 1991), (2) también tiene un efecto adverso sobre la eficiencia de los procesos pirometalúrgicos (Ahmadi et al., 2012), (3) la combustión de carbón que contiene pirita puede conducir a la liberación de dióxidos de azufre que causan lluvia ácida (Cheng et al., 2013) y (4) en la flotación de minerales base conlleva un alto consumo de cianuro de sodio y cal, incrementa los costos y los riesgos.
Por lo tanto, existen importantes ventajas de separar la pirita de minerales valiosos en una etapa temprana de procesamiento. Por estas razones, son muy importantes los depresores de piritas, sin embargo, en la literatura existe una gran diversidad de ellos por lo que el mecanismo de depresión es diverso, por ejemplo, pueden funcionar para remover el colector o el activador de la superficie de la pirita, desactivar los iones activadores, evitar la adsorción del colector en la pirita, o hacer que la superficie de la pirita sea hidrófila. Una de las alternativas que se pretende estudiar es el uso de biopolímeros modificados que son extraídos de la corteza de madera, con esto se busca sustituir reactivos contaminantes y económicamente poco atractivos por reactivos sustentables para la depresión de pirita en circuitos de flotación de Zn y Cu. En este trabajo de investigación se presentan los resultados de estudios fundamentales como adsorción y microflotación con minerales puros para después llevar dicho conocimiento a la industria. Derivado de los estudios fundamentales se presentan los resultados obtenidos con minerales de diferentes unidades mineras de México.
Metodología
Materiales
En esta investigación se utilizaron especímenes naturales de pirita de Guanajuato, México y calcopirita y esfalerita obtenida de Ward´s Natural Science Establishment, Inc. E.U.A. procedentes del estado de Durango, México. Las piezas masivas fueron trituradas y purificadas manualmente con un microscopio óptico para eliminar impurezas como calcita, silicatos y otros sulfuros. Además, se utilizaron dos muestras cabeza de flotación de dos unidades mineras ubicadas en México.
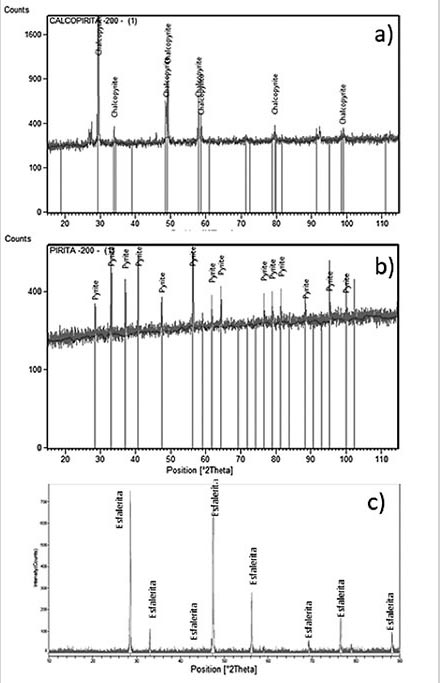
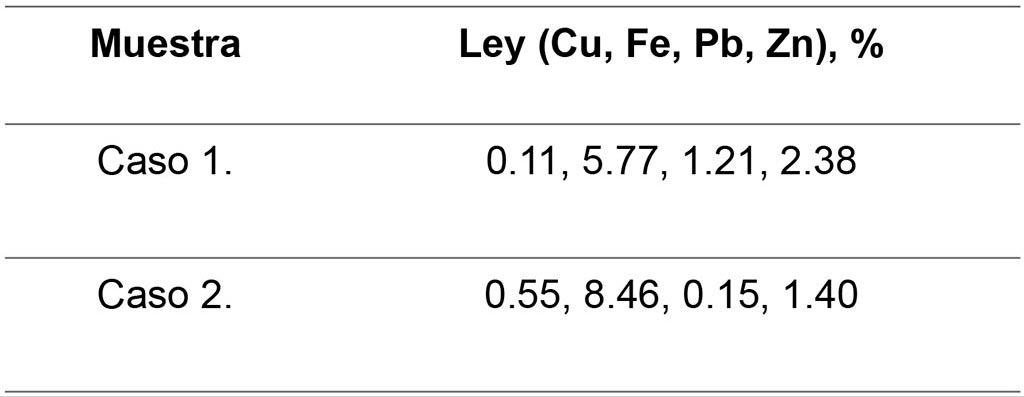
Las muestras puras de pirita, calcopirita y esfalerita se trituraron con un mortero de ágata y se tamizaron para obtener la fracción de tamaño -100+75 µm y -38 µm para los estudios de microflotación y adsorción, respectivamente. Las muestras de microflotación fueron caracterizadas mediante difracción de rayos X (XRD). Los difractogramas se muestran en la Fig. 1. Los difractogramas sólo muestran los picos característicos de calcopirita, esfalerita y pirita. No se identificó ninguna otra fase mineral. Por otro lado, la Tabla 1 muestra la ley de cabeza de las muestras provenientes de los circuitos de flotación de las unidades mineras, estas muestras fueron utilizadas para realizar una comparación entre el uso de cianuro de sodio/cal Vs el biopolímero en la eficiencia de flotación de los circuitos de Cu y Zn.
Estudios de microflotacion y adsorción
Los estudios de microflotación se llevaron a cabo utilizando un tubo Hallimond. Se utilizó un gramo de mineral puro a tamaños -100+75 micrómetros en una suspensión de 100ml de agua desionizada. El pH de la pulpa fue ajustado con la adición de soluciones acuosas de HCl y NaOH, después se añadió el depresor biopolímero F-250 (Pionera) a dosificaciones 1,5, 10, 20 y 30 ppm y se puso en contacto por 10 minutos. Después, se añadió PAX a una concentración de 1X10-3M y se dejó reaccionar por 5 minutos. Finalizado el acondicionamiento, las muestras fueron transferidas al tubo Hallimond y se flotaron por 1 minuto utilizando un flujo de nitrógeno ultrapuro de 30ml/min. La recuperación fue calculada por diferencia de peso.
Para el estudio de adsorción del biopolímero F-250 sobre los minerales se utilizó 1g del mineral a -38 micrómetros, se acondicionó en una solución acuosa de 100ml a un pH deseado y a una concentración de 10, 20, 40, 50, 75 y 100 ppm del biopolímero F-250. El biopolímero y el mineral se dejaron reaccionar durante 10 minutos. Finalizado el periodo de acondicionamiento, la pulpa se filtró utilizando papel filtro poro cerrado y la solución libre de sólidos se analizó químicamente para determinar la concentración residual del biopolímero. Se determinó la densidad de absorción sobre los minerales por diferencia entre la concentración inicial y la residual. La determinación del polímero en solución se realizó utilizando la técnica de espectroscopia de luz ultravioleta-visible (UV-VIS) a una longitud de onda de 300 nm (Mu et al., 2016).
Pruebas de flotación de laboratorio
Para determinar la respuesta a la flotación se utilizó una celda de flotación marca Denver. Durante las pruebas de flotación se determinará la cinética de flotación del Zn, Cu y Fe en función del pH de la pulpa y adición del biopolímero F-250. La cantidad de reactivos se determinará en función de la comparación con el esquema químico que actualmente tiene cada unidad minera. Los resultados obtenidos se evaluarán mediante curvas grado-recuperación las cuales indicarán la máxima flotabilidad y calidad de los productos obtenidos.
Resultados
Estudios fundamentales: Adsorción y Microflotación de pirita, calcopirita y esfalerita utilizando el biopolímero F-250
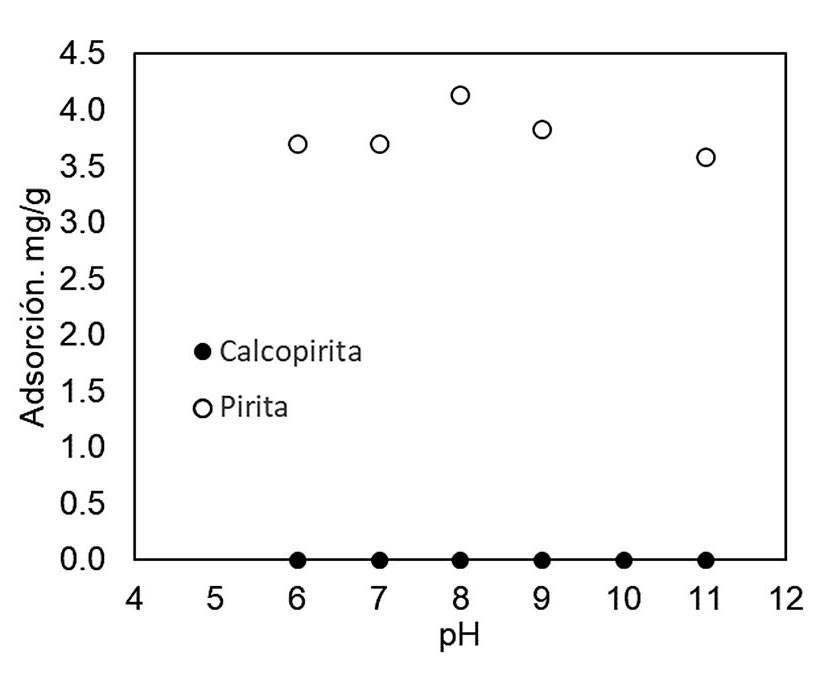
Una de las primeras condiciones de este proyecto de investigación es determinar que exista interacción entre el biopolímero F-250 y los minerales de interés. Para esto, se realizaron pruebas de adsorción utilizando minerales puros. La Figura 2 muestra la adsorción del biopolímero sobre pirita y calcopirita, donde se observa que el mineral de ganga, en este caso la pirita, tiene una alta adsorción por el biopolímero, caso contrario a la calcopirita donde no se aprecia adsorción. Además, es muy claro que la adsorción del biopolímero sobre pirita será muy buena en todo el rango de pH. El hecho que el biopolímero se adsorba de forma selectiva en el mineral de ganga permite inferir una buena separación por flotación al utilizar el biopolímero como depresor.
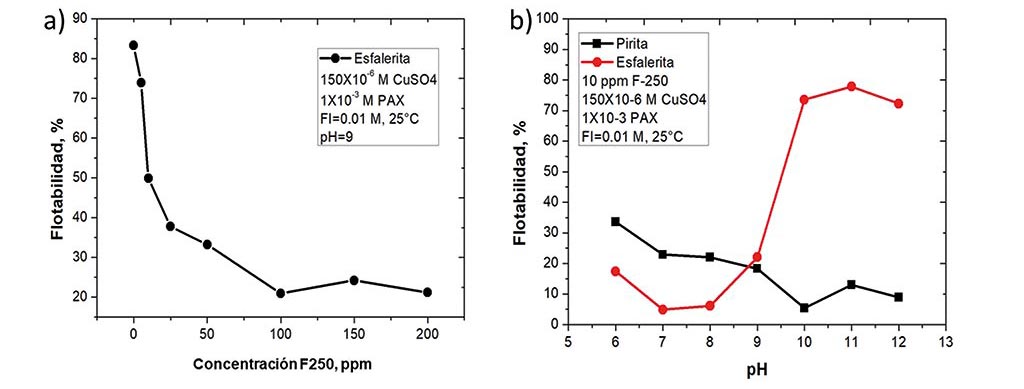
Para fortalecer la evidencia de uso de biopolímero no sólo en la flotación de calcopirita, también se muestra los resultados de flotación de esfalerita. Para esto, se realizaron pruebas de micro flotación en función del pH y la concentración del biopolímero en presencia de xantato amílico de potasio. Las figuras 3 y 4, presentan la comparación de flotabilidad de esfalerita, calcopirita vs pirita en función del pH y la concentración del F-250.
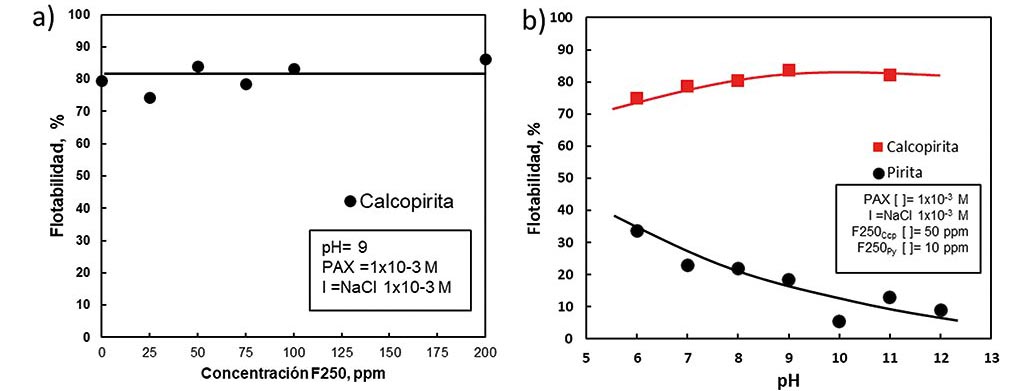
amílico de potasio. a) Flotabilidad de calcopirita en función de la concentración de F-250; b) Flotabilidad
de calcopirita y pirita en función del pH.
La Fig.3a muestra que el F-250 permite que la esfalerita flote a pH de 9 siempre que la dosificación del biopolímero sea inferior a 10ppm. Por el contrario, cuando la concentración es superior a 10ppm se empieza a deprimir la esfalerita. En la Fig.3b se observa la comparación de flotación de pirita vs esfalerita en función del pH a una dosificación de 10 ppm de F-250, donde el gráfico muestra claramente que se puede establecer una zona de separación selectiva en función del pH. Valores de pH inferiores a 9, se tendrá una depresión de los dos minerales, por el contrario, valores del orden de 10 se tendrá una excelente selectividad. Esta gráfica permite ver la región donde el biopolímero se adsorbe sobre cada mineral.
La Figura 4a muestra que el F-250 no deprime a la calcopirita en todo el intervalo de concentración utilizado. A diferencia de la pirita y la esfalerita, donde se requiere alrededor de 10 ppm para deprimir su flotación. Estos resultados concuerdan con la Fig.2 donde no se registró adsorción del biopolímero en la superficie de calcopirita. La Fig.4b muestra la comparación de flotación entre pirita y calcopirita en función del pH donde se puede observar que en todo el intervalo de pH se logra una separación efectiva entre estos dos minerales.
Los resultados de adsorción y microflotación permiten ver que el F-250 es más efectivo para deprimir la flotación en el siguiente orden pirita>Esfalertita>>> Calcopirita. Estos resultados permiten ver el potencial del F-250 en el control de la pirita en los diferentes circuitos de flotación, remarcando que no es necesario tener valores de pH mayores a 10.5 o superiores como se presentan en algunas unidades mineras. Particularmente, para el caso del Zn, si se requerirá tener un buen control de la adición de F-250 y el pH de la pulpa para lograr una separación selectiva entre la pirita y esfalerita.
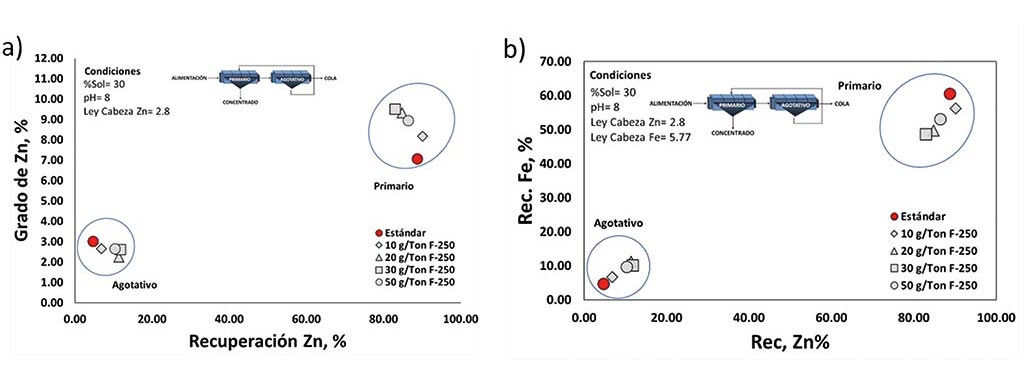
función de la dosificación de F-250.
Caso de estudio 1: Flotación en Circuito de Zinc, 2.8%Zn
Se tiene un mineral con una ley de cabeza de 2.8% Zn, el circuito de flotación industrial cuenta con una etapa de flotación primaria y una agotativa, donde el concentrado agotativo retorna al primario y el concentrado primario va a hacia las limpias de Zinc. En este mineral, se evaluó la adición del biopolímero F-250 utilizando dosificaciones de 10, 20, 30 y 50 g/ton, además se realizó una comparación versus el esquema de flotación utilizado en la unidad minera, la cual será llamada prueba estándar.
La Figura 5a muestra la curva grado-recuperación de Zn, donde se aprecia particularmente para el primario, que la mayoría de los puntos que corresponden a la adición del F-250 resultó en una mejor eficiencia con respecto a la prueba estándar. La mejora en el grado de Zn fue del orden de 1-2% para las diferentes dosificaciones.
La Fig.5b muestra la selectividad entre el Zn y el Fe, donde se puede observar como la prueba estándar tuvo una mayor recuperación de Fe en el concentrado primario. Por otro lado, el F-250 tiene una tendencia marcada con respecto al incremento en la dosificación, es decir, una concentración alta de F-250 disminuye considerablemente el contenido de Fe, pero también afecta la recuperación de Zn. En este caso, la dosificación que mostró una mejor eficiencia en comparación con la estándar fue de 10 ppm. Es importante remarcar que la flotación se llevó a pH de 8, por lo que se espera una mejor eficiencia en la selectividad utilizando un pH superior a 9 como se mostró en las pruebas de microflotación.
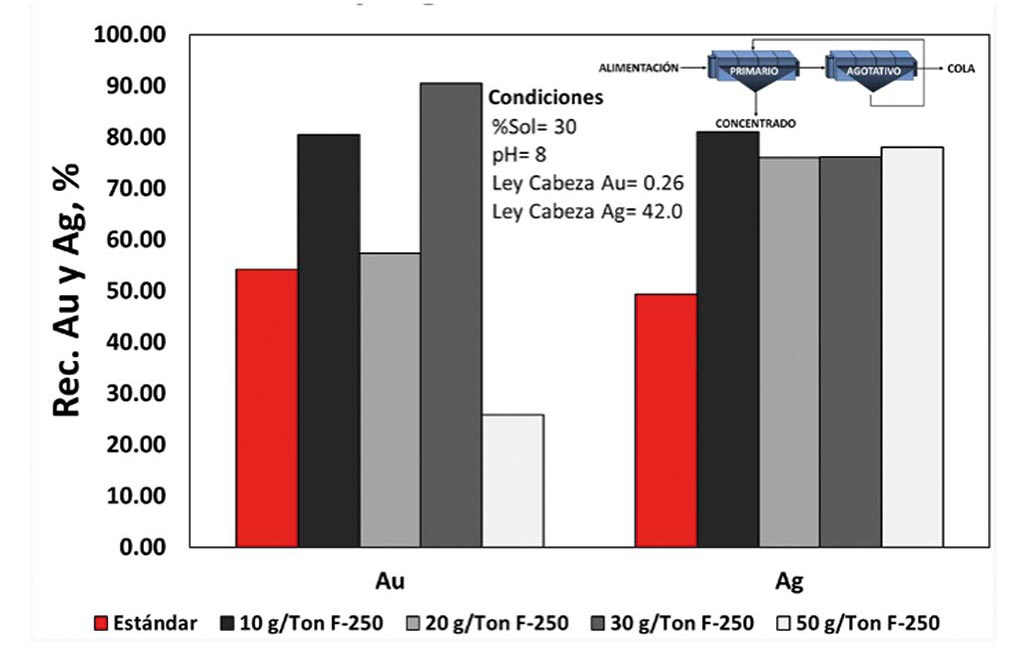
Además de la selectividad sobre el Fe, se analizó el efecto sobre los elementos preciosos Au y Ag. La Figura 6 muestra la recuperación de Au y Ag para la prueba estándar y las diferentes dosificaciones de F-250 estudiadas. La recuperación de Ag mostró un efecto positivo con la adición del F-250, siendo un 20% superior a la prueba estándar en todas las adiciones del F-250. En el caso del oro, tenemos un efecto también positivo para concentraciones de 10, 20 y 30 g/ton, sin embargo, para concentraciones altas (50g/ton) tenemos una disminución de la recuperación de Au, la cual pudiera estar relacionada a la depresión de piritas asociadas con Au.
Caso de estudio 2: Flotación en Circuito Pb-Cu-Zn
Se tiene un mineral con una ley de cabeza de 0.15%Pb, 0.55%Cu, 1.16% Zn y 8.40% Fe, el circuito de flotación industrial está constituido por una flotación Pb-Cu para después flotar el Zn en un segundo circuito. En este mineral se evaluó la adición de 55g/ton biopolímero F-250 sobre la cinética de flotación, utilizando tiempos de 1, 2.5, 5 y 10 minutos de flotación en el primario. Además, se realizó una comparación versus el esquema de flotación utilizado en la unidad minera, la cual también será llamada prueba estándar. Durante este estudio también se evaluó el tiempo de acondicionamiento y la opción de añadir el F-250 en la etapa de molienda.
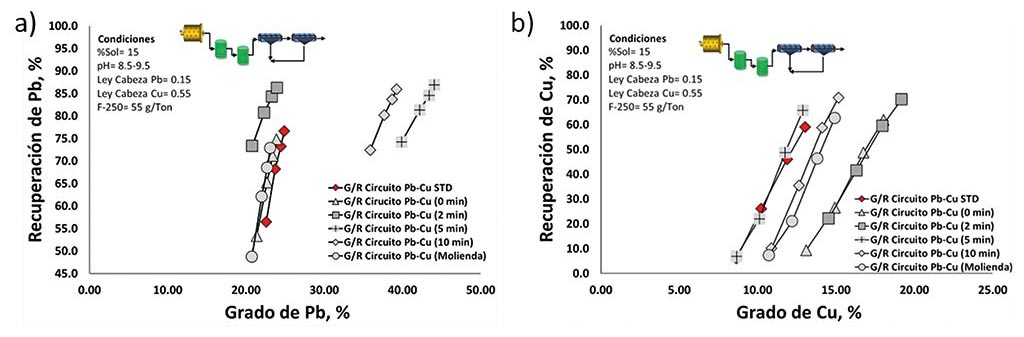
En la Fig.7a se muestra que para las pruebas con 0, 2 minutos y la adición en el molino la respuesta en la eficiencia de flotación fue inferior a la prueba estándar. Por el contrario, la eficiencia en la flotación de plomo se observó beneficiada cuando el tiempo de acondicionamiento fue de 5-10 minutos, mejorando tanto el grado como la recuperación de plomo. Para el caso del Cu (Fig.7b), se puede observar que en la mayoría de las condiciones estudiadas se superó la prueba estándar, mostrando la excelente selectividad entre calcopirita y pirita al utilizar el F-250 descrito con anterioridad. Es importante describir que la idea de usar bipolimeros tiene como objetivos, utilizar pH bajos, disminuir el consumo de cal y disminuir el uso de reactivos como el NaCN, por lo que el F-250 muestra buenos resultados compitiendo con el esquema convencional.
En este ejemplo, una vez recuperado en Pb-Cu, se tiene la flotación de Zn donde se busca disminuir el Fe en el concentrado final. Las colas finales del Pb-Cu se les añadió una dosificación de 10g/ton de F-250 y se realizó la comparación con el esquema convencional. Es importante mencionar que en el esquema convencional normalmente se está realizando a pH superiores a 10.5 para el control del Fe.
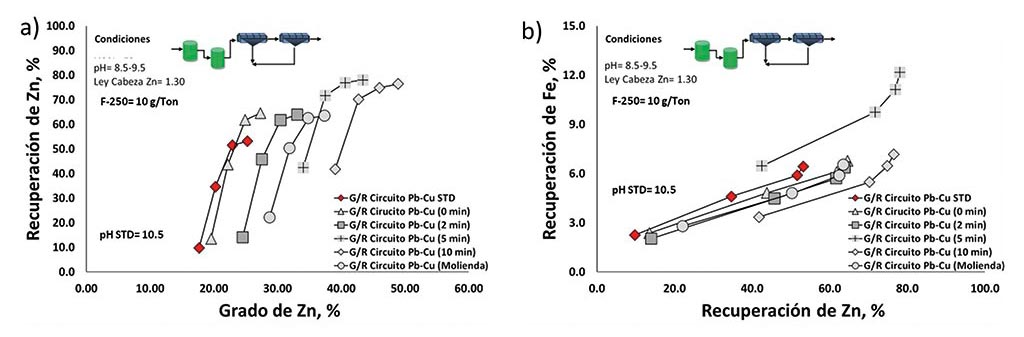
La Fig. 8 muestra como en todas las pruebas donde se añadió el F-250, se tiene un efecto positivo de desplazamiento de la curva grado recuperación, resultando en una mejor recuperación y un mejor grado Zn en el concentrado primario. Por ejemplo, para los 10 minutos de flotación en el primario la prueba estándar alcanza recuperaciones del orden de 55%, por el contrario, en el esquema donde se usa el F-250 se alcanzaron recuperaciones de 78%, siendo muy superiores a la prueba estándar. En el caso de la selectividad Fe-Zn, se puede apreciar como la prueba estándar tiene un menor desempeño en la separación, inicialmente, debido a que merma la flotación de Zn como ya se mencionó y en segundo, porque presenta recuperaciones de Fe más altas que cuando se usa el F-250. Estas mejoras en la recuperación de Zn pueden estar atribuidas al cambio de pH y a la sustitución del complejo Zn/CN.
Conclusiones
- El biopolímero F-250 presenta una buena adsorción sobre el principal mineral de ganga, la pirita. Además, se encontró que la efectividad del biopolímero sobre pirita no es dependiente del pH y puede ser utilizado en el intervalo de 6-11.
- Con base en los estudios de adsorción y microflotación se demostró que el F-250 tiene un excelente rango de selectividad para deprimir la pirita en comparación con la calcopirita y esfalerita, siendo más fácil la separación entre pirita-calcopirita que pirita-esfalerita. La separación de pirita-esfalerita es muy dependiente de las condiciones de pH.
- En las muestras reales provenientes de las unidades mineras, el F-250 mostró una excelente competitividad contra los esquemas químicos convencionales, inclusive mejores resultados para el control de la flotación de los minerales portadores de Fe. Además, el F-250 demostró que es posible deprimir el Fe a pH inferiores a 10.5 en los circuitos de Pb, Cu y Zn.
Referencias
- Ahmadi, A., Ranjbar, M., & Schaffie, M. (2012). Catalytic effect of pyrite on the leaching of chalcopyrite concentrates in chemical, biological and electrobiochemical systems. Minerals Engineering, 34, 11–18. https://doi.org/10.1016/j.mineng.2012.03.022
- Cheng, H., Liu, Q., Huang, M., Zhang, S., & Frost, R. L. (2013). Application of TG-FTIR to study SO2 evolved during the thermal decomposition of coal-derived pyrite. Thermochimica Acta, 555, 1–6. https://doi.org/10.1016/j.tca.2012.12.025
- Mu, Y., Peng, Y. & Lauten, R. A. (2016b). The mechanism of pyrite depression at acidic pH by lignosulfonate-based biopolymers with different molecular compositions. Minerals Engineering, 92, 37 46
- Wang, X. H., & Eric Forssberg, K. S. (1991). Mechanisms of pyrite flotation with xanthates. International Journal of Mineral Processing, 33(1–4), 275–290. https://doi.org/10.1016/0301-7516(91)90058-Q
1Departamento de Ingeniería en Minas, Metalurgia y Geología de la División de Ingenierías Campus Guanajuato de la Universidad de Guanajuato, ExHacienda de San Matías S/N, Colonia San Javier, C.P. 36020, Guanajuato, Gto.
2KOPRIMO materias primas para la Minería, José Maria Velazco 34, Colonia San José Insurgentes, Delegación Benito Juárez, C.P. 03900, CDMX.




















