Caracterización electroquímica de material carbonoso para procesos adsortivos
Josué Manuel Perea Jiménez1 y Lucía Guadalupe Alvarado Montalvo2
Resumen
En el presente trabajo, se realizó una caracterización fisicoquímica y electroquímica de un carbón activado comercial, para así evaluar su capacidad de adsorción y electro-adsorción, además de sentar bases sobre la posibilidad de utilizar dicho material como electrodo para el tratamiento de efluentes. Siendo la electro-adsorción una adsorción inducida por una diferencia de potencial entre un sistema de electrodos, este principio fue utilizado para la caracterización de material carbonoso mediante su aplicación como adsorbente de sales, en este caso NaCl, sobre carbón activado y así estudiar ambas capacidades.
Abstract
In this work, a physicochemical and electrochemical characterization was done on the commercial activated carbon surface, to evaluate its adsorption and electro sorption capacities, and so, lay the groundwork about the possibility of use this material as electrode for the effluents treatment. Electro sorption is a kind of induced adsorption promoted by an electric potential gradient between an electrodes system, this principle was used to do the characterization of the carbon material, applying this technique during the adsorbing of salts, in this case NaCl, on activated carbon and so to study both capacities.
Palabras Clave: Adsorción, Electro-adsorción, carbón activado.
Introducción
En la actualidad, la normatividad gubernamental establece implícitamente el requerimiento de tratamiento de efluentes generados por la industria, de tal manera que ésta reduzca la cantidad y toxicidad de sus residuos y a la vez, se minimice el riesgo que representan para el ecosistema (Tabti et al. 2014). Lo anterior, implica la necesidad de trabajar en el desarrollo de investigación orientada al diseño de materiales, además de técnicas que ayuden en la eliminación de contaminantes presentes en el agua, como por ejemplo, metales pesados y sales. Para dicho fin, una amplia gama de métodos físicos, químicos y fisicoquímicos han sido desarrollados, siendo la adsorción con carbón activado, uno de los métodos más tradicionales, debido a su alta eficiencia y bajo costo.
Se sabe que el carbón activado es un material con una gran área superficial, lo que permite una alta capacidad para adsorber materiales presentes en líquidos y gases; además, ya que se trata de un material no selectivo a especies orgánicas e inorgánicas, es posible emplearlo para la eliminación de más de una especie a la vez, lo que lo hace versátil para una amplia gama de posibilidades de aplicación (Piwek, J.). Si bien, la estructura del carbón activado permite la adsorción superficial de especies, su desorción requiere de nuevas condiciones, cambio de temperatura o el uso de una solución con la que el sustrato entre en contacto, de tal manera que permita una elución (siempre y cuando haya una adsorción física) (Hou, C.). Sin embargo, realizar un proceso de electro-adsorción permite que se pueda aplicar un campo eléctrico, el cual, una vez terminado el proceso, sea invertido para obtener la desorción del ion. Al aplicar un campo eléctrico entre dos electros, los iones parte de la solución serán forzados a desplazarse hacia el electrodo de carga opuesta, lo que da lugar a la separación iónica (Bard et al. 2001).
Así, el objetivo general del presente proyecto es la caracterización de carbón activado, evaluando su potencial para para ser aplicado en sistemas de adsorción y electro-adsorción, evaluando su capacidad de adsorción libre e inducida mediante la aplicación de un campo eléctrico externo.
Metodología
Adsorción. Primero se realizaron pruebas para determinar la cantidad de carbón activado marca Hycel necesaria para realizar las subsecuentes pruebas de adsorción. Esta prueba consistió en variar la masa de carbón en un intervalo de 0.01, 0.02, 0.04, 0.06, 0.08, 0.1, 0.2, 0.4, 0.6 y 0.8 g, mismas que fueron puestas en contacto separadamente con 20 mL de solución de NaCl 1M y agitadas por un periodo de 2 h y filtradas. Al finalizar se determinó la conductividad del filtrado con un medidor de conductividad marca Oakton. Todas las pruebas y análisis fueron llevados a temperatura ambiente.
Una vez que se determinó dicha cantidad, se procedió a realizar pruebas de adsorción para obtener las isotermas y aplicar el modelo de Freundlich y Langmuir manteniendo la cantidad de carbón activado constante (0.01 g) en 20 mL de solución de NaCl a concentraciones 0.1, 0.2, 0.4, 0.6, 1, 1.5, 2 y 3 M en agitación constante durante 2 horas, tiempo necesario para alcanzar el equilibrio tanto en la fase líquida, como sólida.
Electroadsorción. Utilizando una barra de grafito de 5 mm de diámetro, se procedió a fabricar el electrodo para análisis. Se colocó cinta teflón en la zona lateral de la barra cilíndrica con el objetivo de trabajar sólo con el área circular plana expuesta. Esa barra se trabajó como blanco, posteriormente también se le colocó una masa conocida de carbón activado, pegado con solución Nafion (Sigma AldrichTM). Los dos sistemas evaluados se citan a continuación en la Tabla 1.
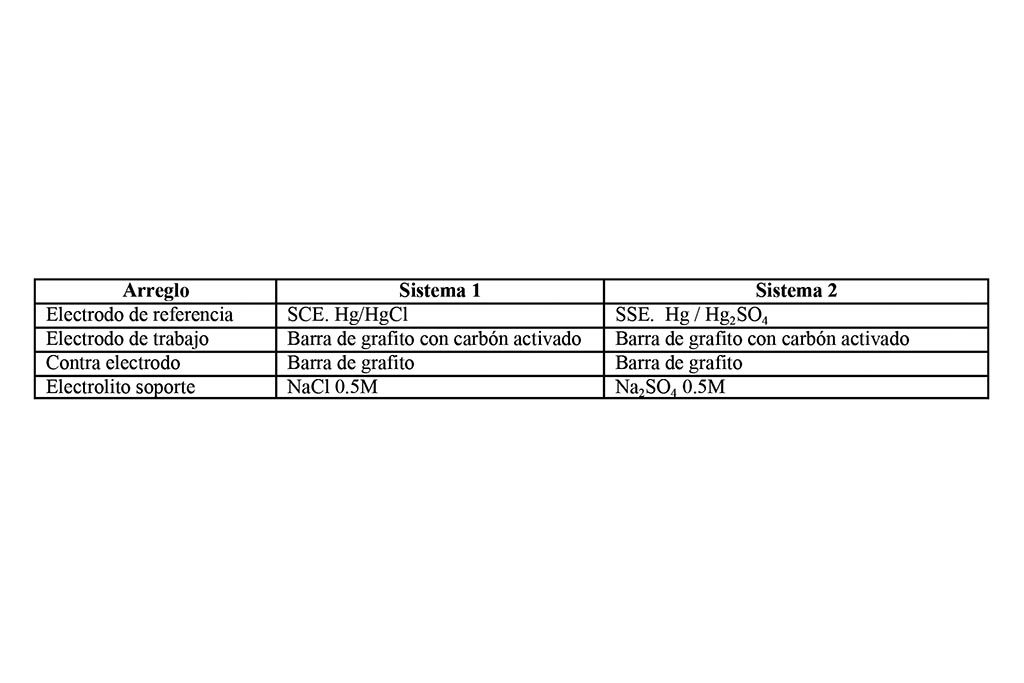
Dichos sistemas se evaluaron en una ventana de -0.25 a 0.75 V vs cada electrodo analizado, a una velocidad de barrido de 50mV s-1 mediante un potenciostato/galvanostato. Estos sistemas se compararon contra un sistema en las mismas condiciones con un electrodo de trabajo que se tomó como blanco: barra de grafito, con diámetro de 5mm.
Resultados
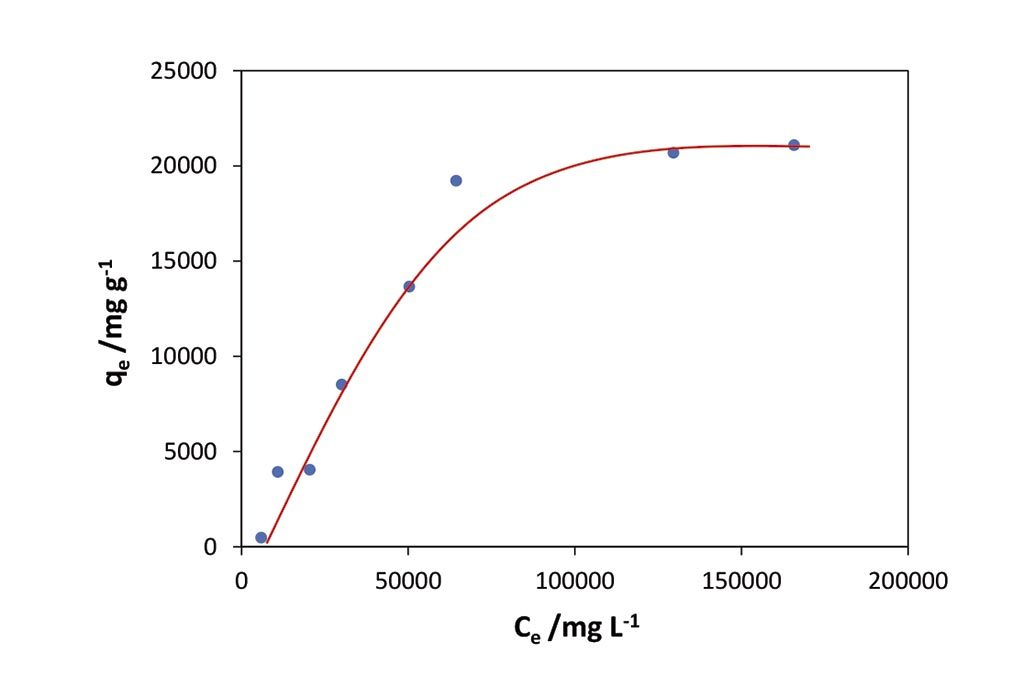
La capacidad de adsorción puede verificarse mediante la Figura 1, donde, a medida que se aumenta la concentración de la solución que entra en contacto con el carbón activado, la adsorción se incrementa. Dichos incrementos son lineales, en los primeros cinco puntos, y más allá de ellos, se observa cómo la pendiente cae, lo que significa que se ha alcanzado la saturación del material, es decir el equilibrio, y por lo tanto, esto es indicativo de su capacidad máxima, que como se puede observar es desde el punto donde se pierde la linealidad del NaCl adsorbido y comienza una línea sin gran pendiente, por lo que se puede ubicar en el gráfico que este es el límite en el cual se satura al material en un rango aproximado a los 20000 mg g-1, observándose como el carbón activado utilizado es capaz de adsorber esta máxima cantidad de adsorbato, por lo que este límite nos ayuda a saber que el CA utilizado tiene este límite de adsorción, el cual es muy alto.
Los resultados de adsorción en base a los modelos de Langmuir y Freundlich, se presentan en las Figuras 2 y 3, respectivamente, donde se puede observar que el ajuste es ligeramente mejor en el modelo de Freundlich, ello significaría que el tipo de adsorción es más del tipo físico, cuestión que favorecería la constante reutilización del carbón. Por su parte, el ajuste al modelo de Langmuir, indica que el proceso de adsorción se da por medio de una adsorción en monocapa, que para este caso fue un poco menor. Tomando en cuenta esta isoterma de Langmuir podríamos estimar que nuestro material tiene 1×106 espacios disponibles para poder adsorber iones de forma independiente. Sin embargo, las correlaciones encontradas ameritan mayores estudios debido a que su correlación para ambos casos fue baja. El efecto de la primera figura indicaría estar orientada al tipo de isoterma favorecida hacia Langmuir.
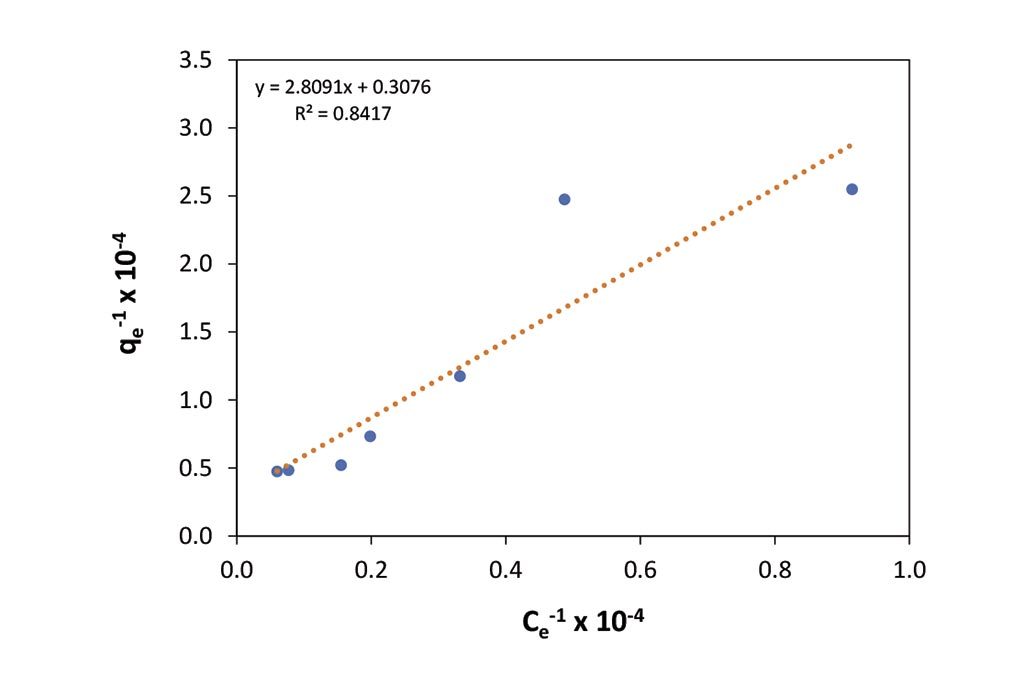
solución de NaCl
En cuanto al proceso de electro-adsorción o electrosorción, como se ha comentado, se exploró una diferencia de campo eléctrico de 1 V en total, para asegurar la no existencia de procesos Faradáicos (transferencia de carga), es decir, garantizar que sólo los procesos no Faradáicos tendrían lugar, como lo son los procesos de adsorción. En las Figuras 4 y 6 podemos observar el aumento de la corriente en la zona de nuestra doble capa eléctrica, por el aumento de material adsorbido entre los dos materiales. En las Figuras 5 y 7 se muestran los gráficos calculados para evaluar la capacitancia con respecto a la ventana de potencial aplicado; como puede observarse, el efecto de la capa de carbón activado, electrodo modificado, muestra una mayor capacidad de adsorción en comparación con la barra de grafito, ya que el aumento de la capacitancia en función del incremento del potencial nos indica su capacidad para adsorber en este caso el cloruro de sodio, al igual que el proceso de desorción, al invertir la dirección de la aplicación de diferencial de potenciales. Para ambos sistemas evaluados se nota alrededor de 400 mF por gramo de carbón utilizado en la adsorción (realizando la diferencia correspondiente con el grafito).
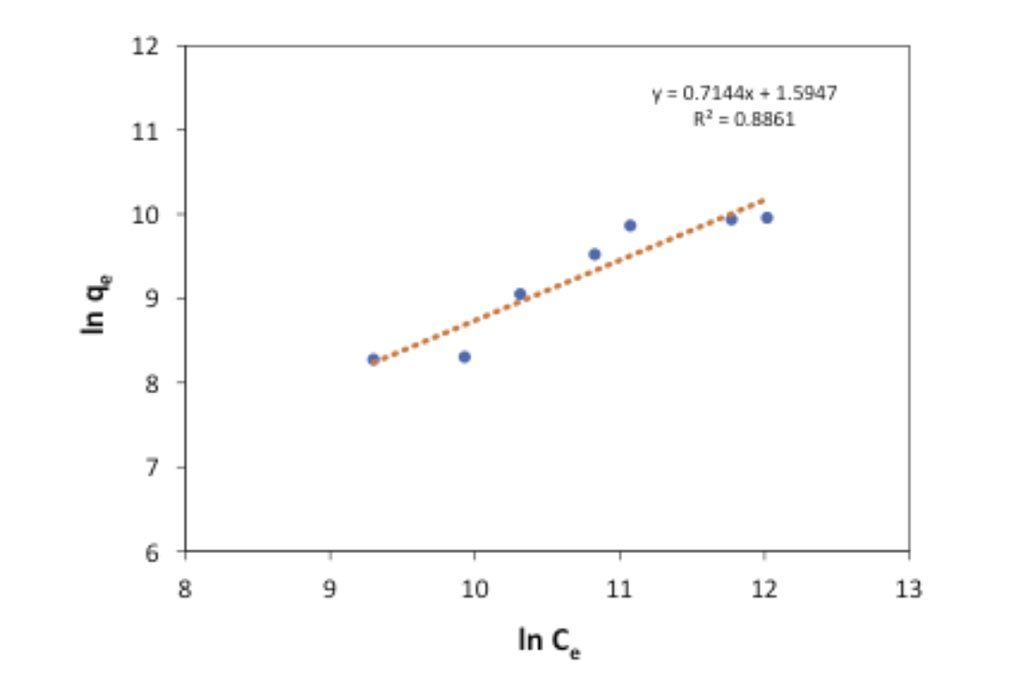
carbón activado
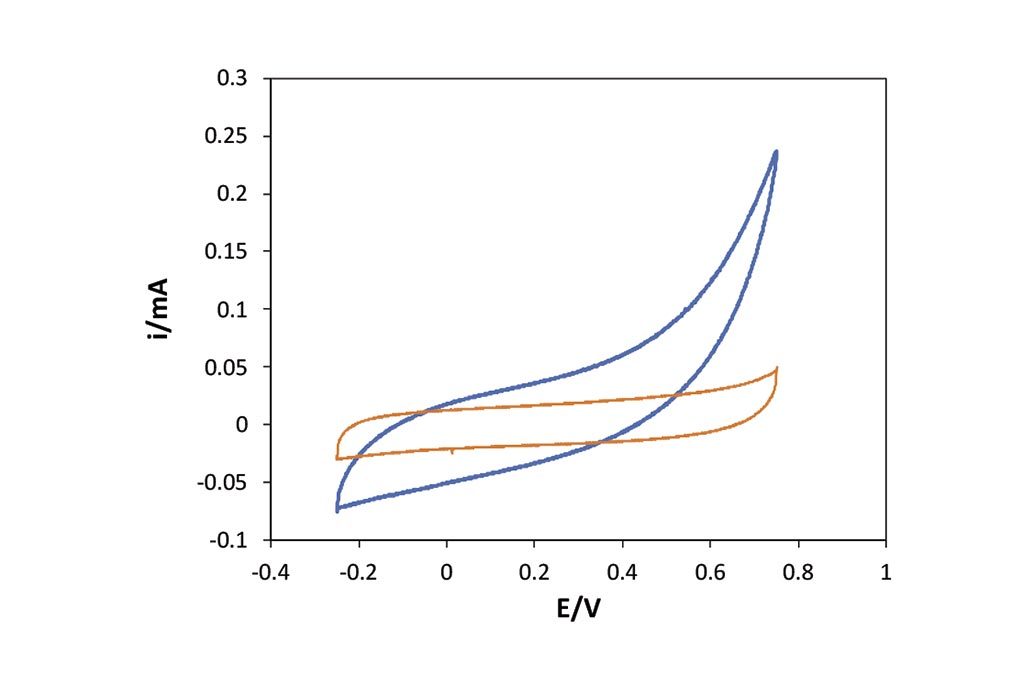
activado (color azul), sistema 2, Tabla 1.
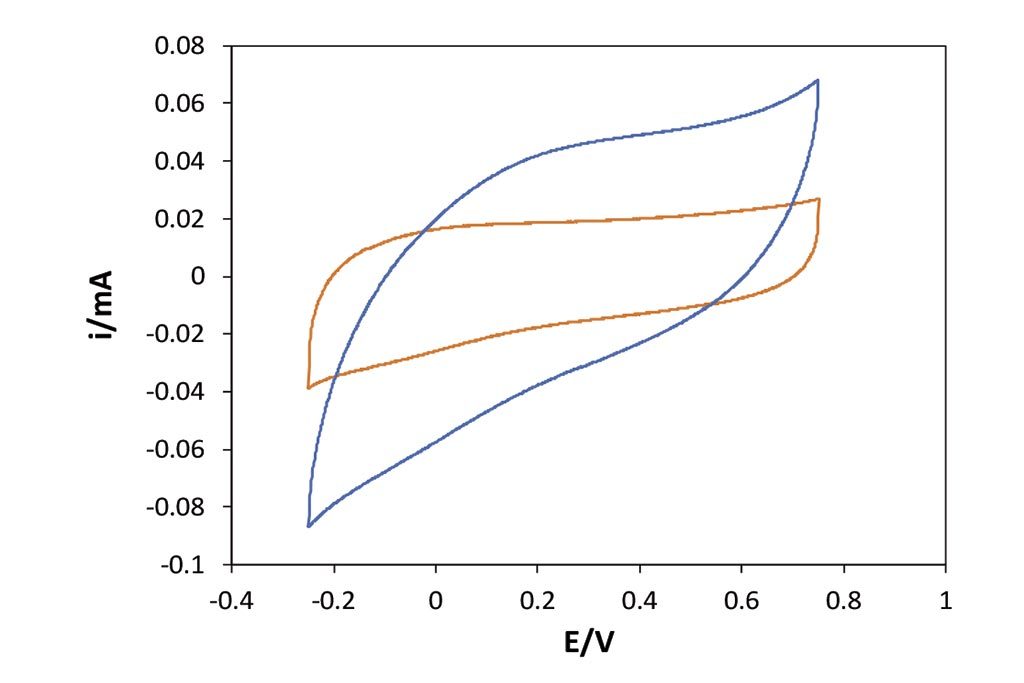
activado (color azul), sistema 2, Tabla 1.
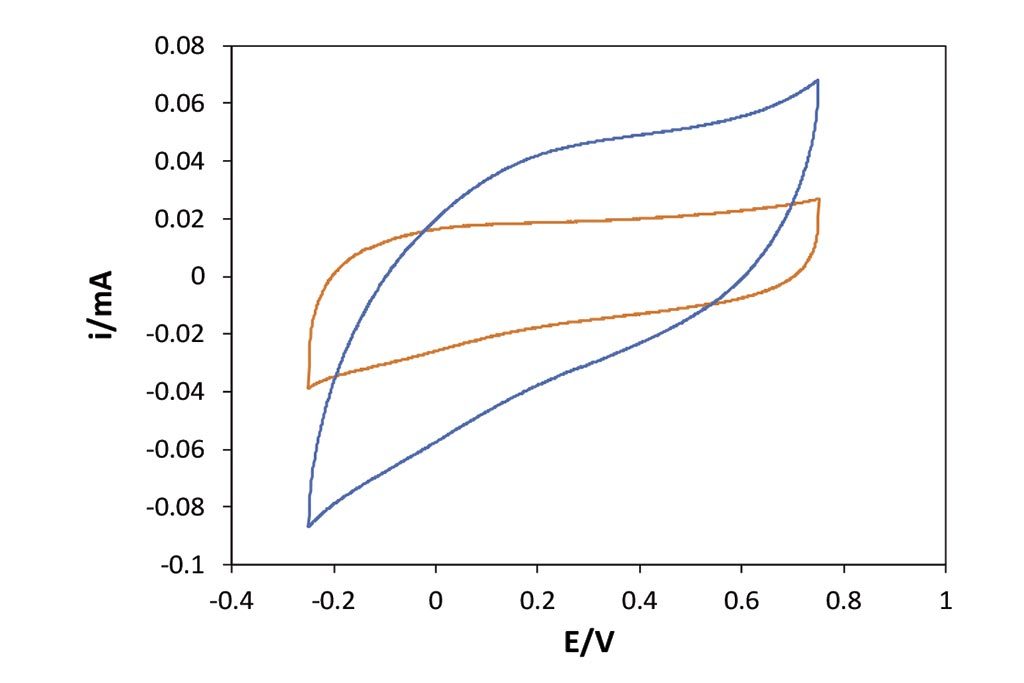
activado (color azul), sistema 1, Tabla 1.
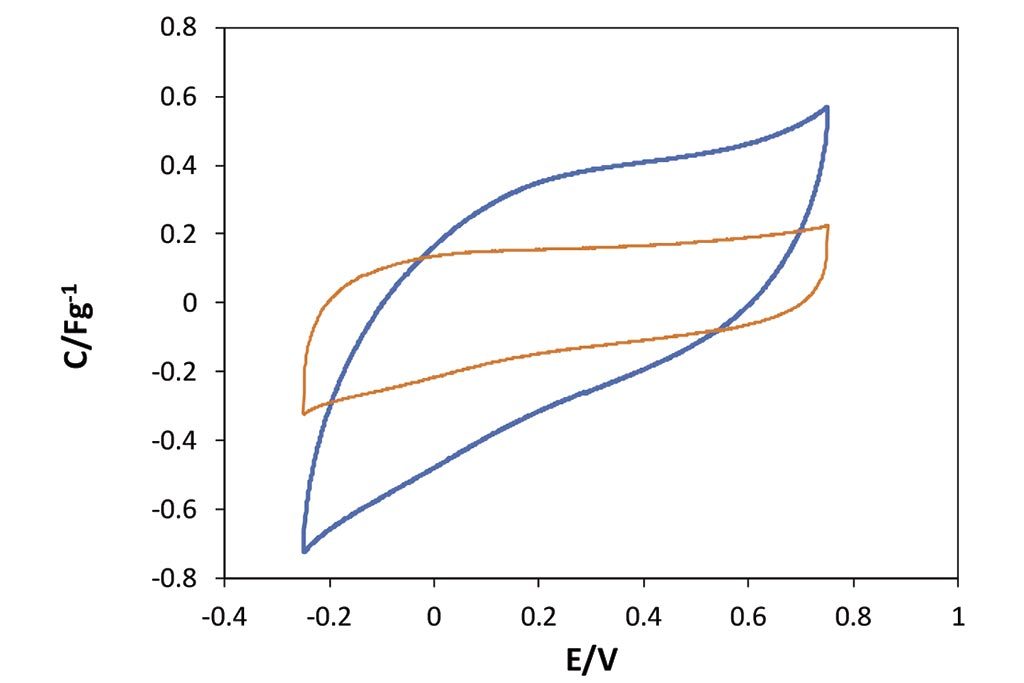
activado (color azul), sistema 1, Tabla 1.
Conclusiones
La ventaja que pueden presentar materiales con capacidad de adsorción en su aplicación para la eliminación de diferentes tipos de especies presentes en medios acuosos, pueden verse beneficiados, ya que una de las ventajas del carbón activado en un proceso de electro-adsorción, es que el material puede ser reutilizado ya que por la aplicación de diferentes potenciales nos ayuda a poder adsorber materiales, como en este caso el cloruro de sodio y desorber al momento de invertir o modificar el potencial, por lo que el uso de este tipo de material para procesos adsortivos en desalinización de aguas, se ve como una práctica viable, por su capacidad de ser reutilizado y el tiempo de equilibrio, que en procesos electroadsortivos se disminuyen por la aplicación del potencial y la generación del campo eléctrico que atrae los iones. Lo anterior, además de la baja energía requerida para el proceso lo hace competitivo para el desarrollo de sistemas de tratamiento en continuo con una regeneración in situ.
Agradecimientos
El estudiante Josué Manuel Perea Jiménez agradece al Comité de Verano de la Ciencia Región Centro la beca otorgada; al Departamento de Ingeniería en Minas, Metalurgia y Geología por las facilidades para el uso de sus laboratorios; al técnico académico Juan Carlos Martínez Barrón por su apoyo en la realización de determinaciones de concentración de especies; al Dr. José Luis Nava y Locksley Castañeda por las facilidades para realizar parte del trabajo en sus laboratorios. Se agradece a la Doctora Lucia Alvarado por su apoyo durante el proyecto y por inspirar en nosotros como estudiantes la labor de la investigación y acercarnos a la ciencia para buscar mejora constante.
1Universidad Autónoma de Querétaro, Facultad de Química, Cerro de las campanas s/n, Centro Universitario, C.P.76010, Querétaro, Qro., jperea29@alumnos.uaq.mx
2 Universidad de Guanajuato, Campus Guanajuato. Departamento de Ingeniería en Minas, Metalurgia y Geología, División de Ingenierías, Sede San Matías, Ex. Hacienda San Matías s/n Fracc. San Javier C.P. 36020, Guanajuato, Guanajuato lucia.alvarado@ugto.mx
Bibliografía
AtkinsJ. de Paula J.. (2008). Química Física. Buenos Aires: medica panamericana.
Bard, A. J. (2001). Electrochemical methods: fundamentals and applications. New York: John Wiley & Sons.
Fethi Bedioui, S. G. (2009). Electroquimica voltametria sobre electrodo sólido. Santiago de Chile: Universidad de Santiago de Chile.
Hou, C. H., & Huang, C. Y. (2013). A comparative study of electrosorption selectivity of ions by activated carbon electrodes in capacitive deionization. Desalination, 314, 124-129.
Piwek, J., Platek, A., Fic, K., & Frackowiak, E. (2016). Carbon-based electrochemical capacitors with acetate aqueous electrolytes. Electrochimica Acta, 215, 179-186.
Tabti Z. (2014). Electroadsorción de plomo sobre carbones activados en diferentes conformaciones: modificación de la química superficial por métodos electroquímicos. 12-08-2018, de Universidad de Alicante Sitio web: https://rua.ua.es/dspace/bitstream/ 10045/41922/1/tesis_zakaria_tabti.pdf



















